-

신소재공학부 구종민 교수
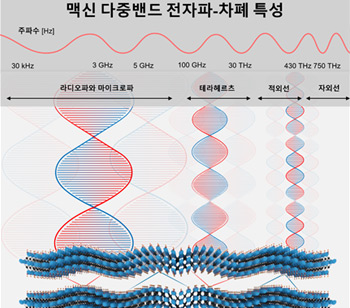
전자파 흡수해 스텔스 기능 갖춘 맥신 소재 개발
신소재공학부 구종민 교수 연구팀은 스텔스* 국방 기술 및 고집적 통신/전자기기의 전자파 차폐 기술에 활용할 수 있는 맥신(MXene) 전자기파 흡수 소재를 개발했다고 4일 밝혔다. * 스텔스기술: 전자기파(波)를 흡수해 레이더 영상에 나타나지 않게 하는 기술로 레이더에 의한 항공기, 미사일의 조기 발견을 곤란케 하는 기술. 전자기파(electromagnetic wave)의 흡수 소재 개발은 레이더 탐지를 무력화하는 스텔스기술 및 통신/전자기기에서 발생하는 유해 전자파 차단·제거를 위해 꼭 필요한 기술로 많은 주목을 받고 있다. 현재 국내 스텔스 전투기 도료기술은 많은 부분을 해외에 의존하고 있어 이에 관한 연구와 개발이 필요하며 고집적 전자장치용 전자파 흡수 소재 개발을 위해서는 가볍고 얇으면서 코팅 가공성이 우수한 소재 기술 개발이 필요하다. 이에 구종민 교수 연구팀은 맥신(MXene) 이차원 나노소재와 ZIP(zeolitic imidazolate framework) 나노소재의 자기조립 구조체를 이용하여 효율적인 스텔스 성능과 전자파 흡수 특성을 가지는 소재를 개발하였다. 맥신 소재 (MXene)는 Ti(티타늄), V(바나듐), Mo(몰리브덴) 등과 같은 전이금속(M)과 질소 또는 산소 원소 (X)을 포함하는 전이금속탄화물 또는 질화물 (Mn+1Xn, n=1=4) 이차원 소재로 전기전도성이 매우 우수한 특성을 가진다. 또한 다량의 표면작용기가 존재하여 표면 음전하 특성을 보이는 나노소재이다. 반면 ZIP 나노소재는 CO2+와 같은 금속양이온과 2-methylimidazole(Hmim)와 같은 유기분자 음이온으로 형성된 3차원 나노소재이다. 연구팀은 유기분자구조를 조절하여 표면양전하를 띠는 ZIP 나노소재를 제조하였다. 연구팀은 맥신의 표면 음전하 특성과 ZIF 나노입자의 표면 양전하 특성을 이용해 정전기적인력(electrostatic interaction)에 의한 자기조립 하이브리드 나노구조 소재를 제작하였다. 이 소재는 각 나노소재의 상반된(음·양전하) 표면전하특성에 의해 이종계면(heterointeface)에서 매우 강한 내부 전기장(built-in electric field, BIEF)이 형성된다. 이 내부 전기장이 강한 유전손실을 유도하여 X-band (8-12 GHz) 주파수 영역*에서 2.5mm 두께의 스텔스 성능(반사손실 RL)을 보여주었고 47.5dB, 유효밴드범위가 6.3GHz인 우수한 전자파 흡수 성질 및 스텔스 성능을 가진다는 것을 밝혔다. 연구팀은 개발된 맥신 나노소재가 저주파인 라디오파(RF)에서부터, X-band, 테라헤르츠, 적외선에 이르는 광범위한 주파수 영역에서 우수한 전자기파 차폐 및 흡수 성능을 가지는 소재임을 확인하였다. 이를 활용하면 스텔스 응용뿐 아니라 통신/전자소자용 차폐 소재, 적외선 스텔스, 적외선 위조 방지 등 다양한 기술로 활용 가능하다. 구종민 교수는 “맥신 소재는 향후 국내 KF-21 스텔스 전투기 제작사업에서 스텔스 소재로 활용할 수 있으며 그 외에도 최첨단 고집적 전자소재 그리고 전기 자동차의 유해 전자파 흡수 소재로도 활용할 수 있을 것”이라고 설명했다. 과학기술정보통신부의 중견연구자사업, 나노및소재 사업, 출연연융합연구사업과 포스코(POSCO)의 지원을 받아 수행된 이번 연구의 성과는 Advanced Materials(IF: 29.4)와 Nature Reviews Electrical Engineering 저널에 동시에 온라인 게재되었다. 1. Zhenguo Gao, Aamir Iqbal, Tufail Hassan, Shengchong Hui, Hongjing Wu*, Chong Min Koo*, “Tailoring Built‐in Electric Field in a Self‐Assembled Zeolitic Imidazolate Framework/MXene Nanocomposites for Microwave Absorption”, Advanced Materials 2024, 2311411 (https://doi.org/10.1002/adma.202311411) 2. Aamir Iqbal, Tufail Hassan, Shabbir Madad Naqvi, Yury Gogotsi, Chong Min Koo*, "MXenes for multispectral electromagnetic shielding”, Nature Reviews Electrical Engineering 2024, 1, 180-198. [연구그림 1] 맥신(MXene) 이차원 나노소재 구조 및 라디오파에서 적외선에 이르는 광대역 주파수 범위에서 발현되는 우수한 전자파 차폐 효과 [연구그림 2] 맥신-ZIF 나노입자의 자기조립구조 및 형성된 하이브리드 구조의 내부전기장(BIEF) 형성 효과 [연구그림 3] 맥신-ZIF 하이브리드의 계면에 형성된 내부전기장(BIEF) 효과 및 BIEF효과에 의해 유도된 우수한 스텔스 성능
- No. 262
- 2024-04-30
- 1389
-

인공지능학과 박은병, 고종환 교수 ·이주찬 연구원
효율적인 3D 장면 표현 방법 개발
전자전기공학부 및 인공지능학과 박은병, 고종환 교수 연구팀은 복잡한 3차원 장면을 신경망 기반의 새로운 모델 구조를 사용하여 효율적으로 나타내는 두 가지 혁신적인 미디어 표현 기법을 발표했다. 이들의 첫 번째 방법론은 뉴럴 네트워크와 전통적인 자료구조인 그리드 방식의 표현을 융합하는 것이며, 두 번째는 소형화된 3D 가우시안 표현을 통해 장면을 표현하는 기법에 관한 것이다. 1) Coordinate-Aware Modulation (CAM) 3차원 이미지 혹은 비디오 등을 표현하는데 있어서 일반적으로 그리드에서 특징벡터를 추출한 뒤 뉴럴 네트워크가 이를 처리하는 방식이 사용되는데, 본 연구에서 제안하는 방식은 뉴럴 네트워크의 각 레이어 마다 모듈레이션 방식으로 그리드의 특징 벡터를 융합하였다. 기존의 그리드 사용 방식은 큰 용량을 필요로 하는 반면, 본 연구에서는 매우 소형의 그리드를 사용하여 고주파 신호를 효율적으로 표현했다. [그림1] 제안된 CAM 구조 연구팀이 새로 개발한 방식을 이미지, 비디오, 3차원 모델, 3차원 비디오 등 다양한 미디어 데이터에 적용한 결과 그 성능이 매우 우수하며 또한 매우 적은 네트워크의 크기로 우수한 신호 복원 능력을 보여주었다. [그림2] 다양한 미디어 도메인에서의 CAM 구조 적용 방안 [그림3] 다양한 미디어 도메인에서의 성능 비교 평가 2) Compact 3D Gaussian Splatting (C3DGS) 최근 3차원 공간을 3D 가우시안 형태의 포인트로 표현하여 100 FPS 이상의 빠른 렌더링이 가능해 졌지만, 이런 방식의 장면 표현 기법은 매우 큰 저장용량을 필요로 한다. 본 연구에서는 공간을 표현하는 가우시안의 수를 렌더링 성능 감소 없이 획기적으로 줄이는 데에 성공하였다. 또한, 가우시안을 나타내는 새로운 방법론을 제시하여 고성능, 빠른 렌더링 뿐만 아니라 매우 효율적인 저장 공간 요구량을 달성하였다. [그림4] 3D 가우시안 형태로 표현된 장면과 C3DGS 적용 결과 다양한 실제 데이터셋을 통해 이뤄진 성능평가에서, 연구팀이 제안하는 방식은 렌더링 품질 저하 없이 25배 이상의 저장용량 감소와 렌더링 속도 향상을 이뤄냈다. [그림5] 다양한 데이터셋에서의 성능 비교 평가 박은병 교수는 “기존의 방식에서 벗어난 새로운 모델 구조를 사용하여 복잡한 3차원 장면을 효율적으로 표현할 수 있는 방식들을 제안하여, 최근 각광받고 있는 NeRF나 생성 모델 등에 매우 효과적으로 사용될 수 있을 것”이라고 말했다. 연구팀의 첫 번째 연구 결과는 NeurIPS, ICML과 더불어 기계학습 분야 최우수학술대회로 꼽히는 ICLR 2024 (International Conference on Learning Representations)에 게재 승인되었고, 제출된 논문의 상위 6%에 해당하는 Spotlight에 선정되었다. 또한, 두 번째 연구 결과는 컴퓨터비전 분야 최우수학술대회인 CVPR 2024 (The IEEE/CVF Conference on Computer Vision and Pattern Recognition)에 게재 승인되었고, 제출된 논문의 상위 3%에 해당하는 Highlight에 선정되었다. 논문명: Coordinate-Aware Modulation for Neural Fields 연구 홈페이지: https://maincold2.github.io/cam/ 저자: 이주찬 (제1저자, 인공지능학과 석박통합과정), 노다니엘 (인공지능학과 석사졸업, 현 KT), 남승태 (인공지능학과 박사과정), 고종환 (교신저자, 전자전기공학부 교수), 박은병 (교신저자, 전자전기공학부 교수) 논문명: Compact 3D Gaussian Representation for Radiance Field 연구 홈페이지: https://maincold2.github.io/c3dgs/ 저자: 이주찬 (제1저자, 인공지능학과 석박통합과정), 노다니엘 (인공지능학과 석사졸업, 현 KT), Xiangyu Sun (인공지능학과 박사과정), 고종환 (교신저자, 전자전기공학부 교수), 박은병 (교신저자, 전자전기공학부 교수)
- No. 261
- 2024-04-23
- 4386
-

신소재공학부 이재찬 교수 ·정봉욱 연구원
전이금속 산화물에 숨겨진 물질상태 예견 및 구현
신소재공학부 이재찬 교수 공동연구팀은 전이금속 산화물에 숨겨진 물질 상태를 이론적으로 예견하고, 이를 박막 표면에 실험적으로 구현하는 데 성공했다고 밝혔다. 본 연구에서 예견 및 구현한 숨겨진 물질 상태는 전하 질서상으로, 초전도 특성, 거대 자기저항, 다강성 등 중요한 응용 물성을 유도하는 데 있어서 출발점으로 알려져있는 물질 상태이다. 전하 질서상은 지금까지 전이금속 산화물 중 전이금속 양이온의 d 궤도를 전자가 다량 점유하고 있는 경우에 존재할 수 있는 것으로 알려졌으나, 본 연구에서는 전자가 전이금속 양이온의 d 궤도를 가장 적게 점유하고 있는 전이금속 산화물에서도 전하 질서상이 박막 표면에 안정적으로 존재할 수 있음을 이론적으로 예견하고 실험적으로 구현하였다. ※ 전하 질서상(Charge-ordered phase): 전자가 균일하게 분포하는 물질에서 전자가 서로 다른 원자에 국소화 되는 상전이가 일어나 서로 다른 원자가를 가지는 이온들이 일정한 규칙성을 띠고 질서 있게 배열된 물질 상태. 초전도 특성, 자기장 인가에 따라 전기저항이 크게 바뀌는 거대 자기저항(colossal magnetoresistance), 강유전성(ferroelectricity)과 강자성(ferromagnetism)이 동시에 존재하는 다강성(multiferroic) 등 중요한 물성과 연결될 수 있음. 본 연구의 학술적 의미는 전하 질서상의 존재는 원소 주기율표에서의 3d 전이금속 산화물 전 영역에서 발생될 수 있음을 밝혔다는 것이다. 본 연구의 대상인 타이타늄산 스트론튬(SrTiO3)은 대표적인 페로브스카이트 전이금속 산화물로 복합 산화물에서 최초로 초전도상이 발견되는 등 중요한 물성이 발현된 바 있다. 그러나 타이타늄산 스트론튬은 전이금속인 타이타늄의 d 궤도를 점유하고 있는 전자가 다른 전이금속에 비해 가장 적어 상대적으로 전자와 전자 간의 상호작용이나 전자와 격자 간의 결합이 약한 물질로 알려져왔다. 이로 인해 전하 질서상이 존재하기 힘들다고 알려져 있었고, 강상관계 물질로서의 신물성 유도에는 제한적으로 활용되어왔다. ※ 페로브스카이트 전이금속 산화물(Perovskite transition metal oxide): ABO3의 화학식으로 표현되는 페로브스카이트 구조를 가지는 전이금속 산화물. 육면체의 꼭짓점인 A 자리에 원자가가 2+인 알칼리 토금속 혹은 원자가가 3+인 란타넘족 원소의 양이온이, 육면체의 체심인 B 자리에 원자가가 3+ 혹은 4+인 전이금속 양이온이 각각 위치하고, 육면체의 면심에는 산소가 위치하는 구조를 가짐. 체심에 위치하는 전이금속 양이온의 d 궤도가 에너지 띠 구조에서 전도 띠(conduction band)를 형성하며 전자, 격자, 궤도, 스핀 간의 상호작용이 크고 이를 통해 새로운 물성을 유도할 수 있어 널리 연구됨. ※ 강상관계 물질(Strongly correlated materials): 전자, 격자, 궤도, 스핀 간의 상호작용으로 일반적인 도체나 부도체에서 알려지지 않은 새로운 물성을 보일 수 있는 물질. 연구진은 우선 제일원리 계산으로 스트론튬을 란타넘으로 일부 치환해 전자가 도핑된 타이타늄산 스트론튬에서 전하 질서상이 준안정상으로 존재함을 이론적으로 예견하였다. 이후 연구진은 란타넘 도핑된 타이타늄산 스트론튬 박막을 타이타늄산 스트론튬 (001) 기판 위에 원자층 수준으로 제어하며 성장시켰고, 그 결과 박막 표면에서 전하 질서상이 유발되어 박막 내부로 침투하며 안정화되는 것을 실험적으로 확인하고 제일원리 계산으로 설명하였다. ※ 제일원리 계산(Ab-initio calculation): 경험적 수량을 전혀 사용하지 않고 기본적인 물리법칙만으로 물질의 물성을 계산하는 방법. 전자의 파동함수를 나타내는 슈뢰딩거 방정식을 풀어서 물질의 전자구조를 얻고 이를 통해 물질의 물리적, 화학적 물성을 이론적으로 예견함. ※ 준안정상(Metastable phase) 물질: 열역학적으로 에너지가 가장 낮은 안정한 상태로 존재하는 대부분의 물질과 달리, 열역학적 에너지가 안정상 보다는 높지만 안정상으로 변화하는데 필요한 에너지의 양이 커서 비교적 안정한 상태로 존재하는 물질. 이재찬 교수는 “박막 표면을 이용해 준안정상을 안정화하는 본 연구의 접근방식은 추후 초전도, 거대 자기저항, 다강성과 같이 전하 질서상에서 비롯될 수 있는 중요한 물성을 발현시키는 데 있어 플랫폼 역할을 할 것으로 기대된다.”고 설명했다. 본 연구 성과는 종합과학분야 국제학술지 ‘네이처 커뮤니케이션스(Nature Communications)에 2월 8일 게재되었다. ※ 저널명: Nature Communications ※ 논문명: Surface triggered stabilization of metastable charge-ordered phase in SrTiO3 ※ DOI: 10.1038/s41467-024-45342-8 ※ 저자 - 교신저자: 이재찬 교수(성균관대학교 신소재공학부), 엄창범 교수(위스콘신 대학교 매디슨 재료공학과) - 제1저자: 엄기태 교수(성균관대학교 신소재공학과 박사, 현 가천대학교 전자공학부), 정봉욱(성균관대학교 신소재공학과 석박사통합과정) - 공동저자: 오세훈(성균관대학교 신소재공학과, 현 숭실대학교 물리학과), Zhou Hua(아르곤 국립연구소 Physicist), 오상호 교수, 서진솔(이하 한국에너지공과대학교 에너지공학부), 최시영 교수, 장진혁(이하 포항공과대학교 신소재공학과), 최민수(성균관대학교 신소재공학과), 이윤상 교수, 서일완(이하 숭실대학교 물리학과), 이형우 교수, 김영민(이하 아주대학교 에너지시스템학과) 이정우 교수(홍익대학교 나노신소재학과), 이경준(위스콘신 대학교 매디슨 재료공학과), Mark Rzchowski 교수(위스콘신 대학교 매디슨 물리학과) ▲ 스트론튬을 란타넘으로 치환하여 전자 도핑된 타이타늄산 스트론튬 박막 표면에 유도된 전하 질서상의 확인
- No. 260
- 2024-04-09
- 5388
-

기계공학부 김태성 교수 ·석현호 연구원
저온 플라즈마 기반 고성능 플렉서블 에너지 저장 소재 개발
기계공학과/나노과학기술학과/반도체융합공학과 김태성 교수 연구팀과 포항공대 김진곤교수 연구팀, 서울시립대학교 문홍철교수 연구팀은 저온 플라즈마와 열공정의 시너지 효과를 활용하여 유연성 기판에 메조다공성 전이금속 산화물 제작에 새로운 개념의 합성공정 기술을 개발했다고 밝혔다. 메조다공성 금속 산화물 (MMO: Mesoporous metal oxide)는 매우 높은 표면적 및 공극률의 장점을 갖고 있어, 고성능의 에너지 저장/전환, 센서, 촉매 등에 널리 사용되는 물질이다. 하지만, 이것을 합성하기 위해서는 매우 높은 고온의 소결 과정이 필요로 하기 때문에 유연성 기판 위에 직접 합성이 불가능하다. MMO 제조시, 널리 사용되는 소프트 템플레이트 방법은 메조 다공성을 부여하는 유기물 지지체와 무기물 전구체를 자기 조립을 통한 유-무기 복합체를 형성하고, 유기물 지지체 제거와 무기물 전구체의 반응이 필요하게 된다. 지금까지의 이것을 위해서 고온 소결이 불가피했다. 본 연구에서는 저온 플라즈마를 이용하여 합성 온도를 낮추어 이러한 문제점을 해결하였다. 열과 플라즈마의 시너지효과는 다양한 종류의 MMO를 150~200도 정도의 온도에서 빠른 합성이 가능하게 하였다. 아울러, 메조다공성 Vanadium Pentoxide (V2O5)을 폴리이미드 기판에 합성하여, 유연한 에너지 저장 소자를 구현하였다. 저온 플라즈마 기반의 합성기술을 개발한 성균관대 김태성교수는 “플렉서블 기반에 직접 합성하는 방식을 발견한 이번 연구는 스마트 에너지 저장/변환 소자 분야에 새로운 패러다임을 제시할 것”이라고 전했다. 연구결과는 과학기술정보통신부 창의후속연구사업, 과학기술분야 기초연구사업, 그리고 나노 및 소재기술개발사업 (나노커넥트)의 지원으로 수행되었으며 소재과학분야 국제학술지 Advanced Materials에 1월 19일에 게재되었다. ※논문명 : Low-Temperature, Universal Synthetic Route for Mesoporous Metal Oxides by Exploiting Synergistic Effect of Thermal Activation and Plasma ※저자명: 김태성 김진곤 문홍철(교신저자), 김건우 석현호(공동제1저자) ※DOI: 10.1002/adma.202311809 ■ 저온 플라즈마를 활용한 메조다공성 박막 합성 ■ 연구책임을 맡은 기계공학부 김태성 교수(교신저자)와 석현호 박사과정(제1저자)
- No. 259
- 2024-04-01
- 5586
-

식품생명공학과 우한민 교수
바이오파운드리의 효율성 극대화를 위한실험가격지수 개발
식품생명공학과 우한민 교수는 합성생물학의 핵심 제조 기술인 연구실 자동화 기반 바이오파운드리* 기술의 경제적 효율성을 정량화할 수 있는 실험가격지수(Experiment Price Index)를 세계 최초로 개발했다고 밝혔다. * 바이오파운드리: 주문자 반도체 생산시스템과 유사하게, 생물시스템을 디자인하고 자동화 장비를 활용하여 고속으로 합성생물학 부품 및 세포공장을 개발할 수 있는 바이오제조 핵심 자동화 시설 실험가격지수(Experiment Price Index, EPI)는 생명과학 및 생명공학에 사용되는 연구 재료비, 인건비 그리고 실험을 수행하는데 소요되는 실험시간을 샘플의 수에 대한 기하평균이다. 따라서 실험가격지수는 낮으면 낮을수록 효율적이다. 성균관대 우한민 교수는 바이오파운드리의 효율성을 정량할 수 있는 실험가격지수를 수치화함으로써 고가의 자동화 로봇을 이용한 대규모 합성생물학 실험을 경제적으로 설계하고 수행할 토대를 마련하게 되었다. 성균관대 바이오파운드리 연구센터에서 수행한 실험 결과에 따르면 유전자어셈블리와 같은 625개의 합성생물학 실험을 인간연구자와 바이오파운드리의 연구 로봇이 각각 수행하는 경우, 샘플당 연구로봇이 인간 연구자에 비해서 대략 2배 정도의 효율적인 실험가격지수를 가지며 특히 바이오파운드리의 연구로봇은 소요되는 실험시간을 3배 이상 줄일 수 있고 최종적으로 연구로봇은 인간 연구자 3명 이상의 능력을 발휘할 수 있다고 연구팀은 밝혔다. 바이오파운드리 시설이 고도화하면 더 높은 효율의 실험가격지수를 얻게 되므로 향후 예비타당성 조사가 통과된 바이오파운드리 인프라의 경제적인 구축에 기여할 수 있을 것으로 기대된다. 우한민 교수(바이오파운드리 연구센터장)는 “이번 실험가격지수(EPI) 개발을 통해서 바이오파운드리 시설 내 대규모 실험 수행 시 경제성을 미리 판단 할 수 있어서 합성생물학 기반 제품의 상업화를 앞당길 수 있고 EPI가 향후 바이오파운드리 국제 표준으로 자리 잡기를 기대한다”고 설명했다. 한편 이번 연구 결과는 2월 23일 셀(Cell)지가 발행하는 생명공학 분야 권위 저널인 ‘생명공학의 동향(Trends in Biotechnology)’의 온라인판에 게재됐다. 이번 연구성과는 한국연구재단이 지원하는 중견연구자지원, 기초연구실지원사업, 미생물 제어 및 응용 원천기술개발사업 및 과기정통부가 지원하는 석유대체 친환경 화학기술개발사업의 바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발 과제의 지원을 받아 수행되었다. ※ 저널: Trends in Biotechnology(2024), Impact factor 17.3 (2022년 기준), JCR 생명공학 및 응용미생물학 분야 상위 1.6% 저널 ※ 논문제목: Measuring the economic efficiency of laboratory automation in biotechnology ※ DOI: 10.1016/j.tibtech.2024.02.001 ※ 제1저자 및 교신저자: 우한민 교수(성균관대학교 식품생명공학과, 바이오파운드리연구센터, 메타바이오헬스학과) ▲ 실험가격지수를 통한 바이오파운드리 실험의 효율성 정량화
- No. 258
- 2024-03-21
- 7212
-

융합생명공학과 발라찬드란마나발란 교수
인간 RNA 정보에서 바이러스 유발 인산화 및 2'-O-메틸화(2OM) 부위 식별 위한 AI도구 개발
융합생명공학과의 발라찬드란 마나발란 교수가 이끄는 CBBL 연구팀은 인간 RNA에서 바이러스 유발 인산화 부위와 2OM 부위를 식별하기 위한 두 가지 최첨단 AI 기반 도구를 개발했다. 그들의 혁신적인 접근법은 최고 수준의 학술지인 Briefings in Bioinformatics (Impact Factor 9.5 & JCR = 3)에 발표되었다. 1. 메타러닝 접근 방식을 사용한 바이러스 유발 인산화 부위 식별 코로나바이러스(SAR-CoV-2)의 전세계적 확산은 건강에 대한 중요한 우려와 도전을 야기하고 있다. 인산화는 세포내 모든 대사에서 중요한 번역 후 수정 방식 중 하나이며, 해당 인산화 부위의 정확한 식별은 코로나바이러스 감염에 대한 이해와 더불어 코로나19 위기를 완화하는 데 도움이 될 수 있다. 하지만, 관련 기술은 현재 개별 인산화 부위 및 기작들에 대한 국지적 결과만 알려져 있을 뿐, 전반적인 인산화 부위 연구 및 의의에 대한 연구는 태부족한 실정이었다. 이에, 융합생명공학과 전영준 교수, 송민경 교수, 이석찬 교수와 협력하여 메타러닝 접근 방식을 사용한 새로운 MeL-STPhos 예측기를 개발했다 (그림 1). 구체적으로, Nhat Truong Pham(박사 과정 학생)과 Le Thi Phan(박사 과정 학생)은 관련 공공재 데이터를 추출하고 29개의 특성 설명자(feature descriptor)와 14가지의 분류기를 활용하여 각 데이터셋에 대해 대규모 기초 모델(약 400개)을 구축하고, 성능이 가장 좋은 모델을 결합하여 최종 예측을 위한 MeL-STPhos 모델을 구축하였다. 흥미롭게도 MeL-STPhos는 코로나바이러스 뿐만 아니라 다른 바이러스에 의해 발생하는 인산화를 식별할 수 있는 능력을 가지고 있으며, 하나의 세포 특이적 모델은 트레오닌 인산화 부위를 정확하게 탐지하여 여러 모델 활용의 효과를 보여주었다. MeL-STPhos는 두 데이터셋에서 기존에 발표되었던 최고의 예측 모델보다 월등한 성능을 보여주어, 다양한 특성 설명자, 분류기 및 메타러닝 접근 방식을 체계적으로 활용하는 접근 방식의 중요성을 입증했다. 그림 1. 데이터셋 구축, 메타러닝 접근법, 최적의 특성 및 분류기 식별, 웹서버 개발을 포함하는 MeL-STPhos 프레임워크 개요 본 연구는 대한민국 보건복지부(HI23C0701), 한국보건산업진흥원(KHIDI)을 통한 한국보건기술 R&D 프로젝트의 지원으로 수행되었다. 또한, 과학기술정보통신부, 한국연구재단(NRF) (2021R1A2C1014338, RS-2023-00217881 및 2021R1C1C1007833)의 지원으로 수행되었으며, 본 연구결과는 2023년 12월 6일 Bioinformatics Briefings 저널에 온라인으로 게재되었다. (https://doi.org/10.1093/bib/bbad433). 2. 하이브리드 딥러닝 프레임워크를 통한 인간 RNA에서 2’-O-메틸화 (2OM) 위치 식별 2’-O-메틸화(2OM)는 RNA의 가장 일반적인 전사 후 수정으로, RNA 접합, RNA 안정성 및 선천적 면역에서 중요한 역할을 하며 다양한 관련 연구에도 불구하고, 2OM의 화학적 안정성 때문에 메신저 RNA(mRNA)에서 탐지 및 식별하는 것은 어려운 것으로 알려져 왔다. 관련하여, 본 연구팀의 Nhat Truong Pham박사과정 학생은 2OM 부위를 정확하게 식별하기 위한 새로운 하이브리드 학습 접근법 H2Opred(그림 2)를 개발했다. H2Opred는 스택방식의 1D 컨볼루셔널 뉴럴 네트워크 - convolutional neural network(1D-CNN) 블록과 주목 기반 양방향 게이트 순환 유닛-bidirectional gated recurrent unit(Bi-GRU-Att) 블록을 활용하여 모델 구축에 성공하였다. 구체적으로, 1D-CNN 블록은 14개의 전통적 특성 설명자(feature descriptor)로부터 효과적인 특성 표현을 학습하였고, Bi-GRU-Att 블록은 RNA 시퀀스에서 추출된 자연 언어 처리 기반 임베딩 5개로부터 특성 표현을 학습했다. 해당 학습을 통하여 개발된 H2Opred 모델은 다양한 데이터셋에서 뛰어난 성능을 보여주었으며, 기존에 발표되었던 예측모델 및 다른 네 개의 뉴클레오티드 특이 H2Opred 모델들을 크게 능가했다. 그림 2. 데이터셋 구축, 특성 추출 및 모델 구축, 특성 융합 및 웹서버 개발을 포함한 H2Opred 프레임워크 개요 본 연구는 과학기술정보통신부, 한국연구재단(NRF) (2021R1A2C1014338 및 2021R1I1A1A01056363)의 지원으로 및 한국보건산업진흥원(KHIDI)을 통한 한국보건기술 R&D 프로젝트의 지원으로 수행되었다. 본 연구결과는 2024년 1월 4일 Bioinformatics Briefings 저널에 온라인으로 게재되었다. (https://doi.org/10.1093/bib/bbad476). 본 연구진은 관련접근 방식들은 2OM이나 인산화 부위를 식별하는 것에만 국한되지 않고, 펩타이드 치료 기능의 식별 및 유전자 발현 데이터를 사용한 알츠하이머병(AD) 예측을 포함한 다른 연구 영역에도 적용 할 계획을 가지고 후속 연구를 수행하고 있다.
- No. 257
- 2024-03-12
- 5793
-

의학과 이기영 교수 ·신지혜 연구원
새로운 폐암 진행 메커니즘 제시
폐암 발병 및 진행은 유전적 변이 및 다양한 인자들에 의해 유도된다. 케모카인 (Chemokine)과 그 수용체는 종양 세포의 성장과 생존, 그리고 암 발생 및 전이에 중요한 역할을 한다. 특히 CXCL13 (Chemokine ligand 13)과 그와 관련된 수용체인 CXCR5 (Chemokine receptor 5)는 신호 전달 경로를 통해 폐암세포의 전이를 촉진하는 것으로 보고되며, 폐암 발병 및 진행과 관련이 있다. 그러나, CXCR5–CXCL13 작용기전이 폐암 진행을 기능적으로 어떻게 조절하는지에 대한 분자 및 세포 메커니즘에 관한 연구는 미흡하다. 본 연구팀은 폐암 환자 유래의 암 조직 및 정상 조직에서 얻은 유전자 데이터를 활용하여 CXCR5 발현이 폐암 세포에 현저하게 증가되어 있음을 확인하였다. 또한 분자 및 세포 기전 연구를 통해, 폐암 세포에서의 TLR4 (Toll-like receptor 4) 신호에 의한 NF-κB의 활성화를 통해 CXCR5 발현이 증가하는 것을 확인하였으며, 더 나아가 CXCR5–CXCL13 작용기전이 TLR4 신호와의 시너지 효과를 통해 폐암 진행에 기능적으로 관여하는 메커니즘을 처음으로 제시하였다. (그림 1) 세균 또는 바이러스 감염은 암 진행을 유도하는 강력한 요인으로 보고되며, TLR4 및 CXCR5의 발현이 높은 폐암 환자들은 세균 또는 바이러스에 감염이 될 경우 폐암 진행이 더 악화될 것으로 예상된다. 따라서, 본 연구에서의 임상적 비교 결과와 기능적 연구를 통해, 향후 폐암 발병 및 진행에 관한 병리학적 원인 규명 그리고 새로운 항암 치료 전략에 기여하리라 기대하고 있다. 본 연구는 제1저자로 신지혜 학생 (성균관대학교 의과대학 석박통합과정)/ 김미정 박사 (성균관대학교 의과대학 BK21 FOUR 신진연구자)/ 김지영 학생 (성균관대학교 의과대학 석박통합과정)이 연구에 기여하였다. 연구결과는 임상 중개 의학 분야 저명 국제 학술지인 Clinical and Translational Medicine (IF: 10.6)에 게재되었다. 이번 연구성과는 한국연구재단이 지원하는 중견연구자지원 및 기초연구실지원사업을 통하여 수행되었다. 논문명: CXCR5 and TLR4 signals synergistically enhance non‐small cell lung cancer progression. Clin Transl Med. 2024 Jan 18. doi: 10.1002/ctm2.1547. 저자: 신지혜 (제1저자, 석박통합과정), 김미정 (성균관대학교 의과대학 BK21 FOUR 신진연구자), 김지영 (석박통합과정), 이기영 (교신저자, 성균관대학교 의과대학 교수). 그림 1: CXCR5-CXCL13 및 TLR4의 시너지 효과에 의한 폐암 진행 기능 메커니즘 제시
- No. 256
- 2024-02-29
- 5245
-

소프트웨어학과 이지형 교수 ·기계공학부 이은호 교수
AI 딥러닝 이용한 자동차 금형 CAD 설계도면 자동 검도기술 개발
인공지능학과 이지형 교수 연구팀과 기계공학부 이은호 교수 연구팀은 현대기아자동차 프레스금형설계팀, 선행생산기술해석팀과 공동 연구를 통해 ‘딥러닝 기반 금형 CAD 설계도면 자동검도기술’을 개발했고 이를 세계적으로 권위 있는 학술지인 EAAI(Engineering Application of Artificial Intelligence, IF: 8.0, JCR 상위 TOP5 이내)에 게재했다. 최근 제조업 분야 설비의 무인화 및 자동화가 활발히 일어나면서 인공지능과 기계학습 모델의 활용이 중요해지고 있다. 제품 생산 과정에서는 인공지능과 기계학습 기술을 활용하여 제품 결함 탐지 및 제품 판별을 진행하고 있지만, 금형의 설계 과정에서는 복잡한 구조로 인해 아직도 많은 경험을 쌓은 엔지니어가 직접 검도를 하고 있다. 하지만, 엔지니어가 많은 항목들에 대해서 검도를 진행하는 것에 있어서 많은 시간과 숙련도가 요구된다. 이에 연구팀은 인공지능 딥러닝 CNN 모델을 활용하여 3차원 금형 CAD 설계도면에서 각종 결함 판단에 기준이 되는 3차원 레퍼런스를 자동 검출할 수 있는 알고리즘을 개발하였고, 이를 CAD 인터페이스에서 바로 활용할 수 있도록 CAD 연동모델을 개발하였다. 자동 검출 알고리즘에는 Object detection 과 Semantic segmentation 모델을 활용하여 CAD 모델에서 취득한 서로 다른 3차원 레퍼런스의 종류 및 위치를 정확히 검출하였다. 또한, CAD 연동 모델을 통해서 CAD 데이터로부터 이미지 자동 추출 작업 및 CAD 인터페이스에서의 레퍼런스 취출 작업을 자동화하였다. (1)사이드 아우터 레퍼런스 취출 연구 (2)자동차 금형 단면 만족도 평가 모델 (3)자동검도시스템 구조 이지형, 이은호 교수는 "단순한 인공적인 금형 설계 데이터가 아니라, 실제 현업에서 사용되는 복잡한 자동차 금형 CAD 설계 데이터에 대해서 실증한 결과가 휴먼에러(human error)와 비슷한 수준을 보였으며, 이러한 연구결과는 산업현장의 전문가의 노동집약적인 검도비용을 획기적으로 줄일 수 있을 것으로 보인다."고 연구의 의미를 설명했다. 또한, "개발한 지그재그 프로세스 프레임워크는 자동차 금형 CAD 데이터 뿐만 아니라, 다른 설계도면 데이터에 대해서도 확장 적용이 가능할 것으로 보이며, 추후 CAD 설계 데이터 검도 자동화 및 스마트 팩토리 분야에 있어서 중요한 역할을 할 것으로 기대한다"고 말했다. 본 연구는 현대기아자동차 프레스성형설계팀과 선행생산기술해석팀, 한국연구재단(IITP, 2019-0-00421), HPC Support Project의 연구결과로 학습 데이터 수가 적음에도 불구하고, 개발한 방법을 통하여 금형의 설계 과정에서의 적용가능성을 보여주었다. 이번 연구 성과로 자동화 및 제어 시스템과 인공지능 분야 학술지인 EAAI(Engineering Application of Artificial Intelligence, IF: 8.0, JCR 상위 TOP5 이내)지에 1월 1일 온라인 게재되었다. 논문명: Automation of trimming die design inspection by zigzag process between AI and CAD domains 논문링크: https://doi.org/10.1016/j.engappai.2023.107283 저자명: Jee-Hyong Lee, Eun-Ho Lee (교신저자), Jin-Seop Lee, Tae-Hyun Kim (제1저자), Sang-Hwan Jeon, Sung-Hyun Park, Sang-Hi Kim (공동 저자)
- No. 255
- 2024-02-23
- 4863
-

생명물리학과 김인기 교수 ·Aleksandr Barulin 박사
단분자를 실시간 관찰할 수 있는 메타렌즈 개발
생명물리학과 김인기 교수, Aleksandr Barulin 박사 연구팀은 포스텍 기계공학과/화학공학과 노준석 교수, 박사과정 김예슬씨, 오동교씨 연구팀과 공동 연구를 통해 상온에서 단분자(Single molecule)의 움직임을 실시간으로 관찰할 수 있는 초고민감도 메타렌즈(Metalens) 장치를 개발해 세계적인 과학 학술지인 네이처 커뮤니케이션즈(Nature Communications)에 논문을 게재했다. 단분자 감지 기술은 바이오센싱, 화학 분석, 분자 역학, DNA 염기서열 분석 및 정밀의학 분야의 핵심 기술로 여겨지고 있다. 단분자를 검출하기 위한 다양한 방법 중에 가장 많이 사용되는 방법 가운데 하나는 형광 상관 분광 기술로(Fluorescence Correlation Spectroscopy, FCS), 분자에서 방출되는 형광 신호들의 상관 함수를 분석하여 각각의 분자의 거동을 관찰할 수 있다. 특히 FCS 기술은 렌즈의 특성에 굉장히 민감하기 때문에, 현재까지 보고된 대부분의 FCS 기술은 해상도가 높은 고배율의, 수차가 보정된 비싼 대물렌즈를 사용하였다. 현장형 감염병 진단 및 맞춤/정밀의학에 대한 수요가 높아짐에 따라 과학자들은 포터블 형태의 바이오센서 및 스마트폰에 연동 가능한 현미경과 같은 새로운 바이오메디컬 디바이스를 개발하려는 노력들을 해오고 있다. 하지만 현재까지 기존의 대물렌즈를 소형화 할 수 있는 기술의 부재로 초소형 형태의 단분자 진단 기기는 개발되지 못하고 있는 실정이다. 연구진은 머리카락 굵기 1000분의 1에 불과한 초박형 평면 광학 소자인 메타표면을 활용해 단분자의 움직임을 실시간으로 관찰할 수 있는 초고민감도 메타렌즈 장치를 개발했다(그림 1). 단분자 관찰을 위해서는 높은 집광 효율 및 큰 개구수를 가지며, 동시에 수차가 정교하게 보정된 고품질의 렌즈를 사용해야 한다. 연구팀은 이러한 모든 조건을 만족시키는 메타렌즈를 구현하기 위해 실리콘 기반의 나노 구조를 최적화하였고, 정밀한 나노공정을 통해 디바이스를 제작하였다. 연구팀은 제작된 메타렌즈를 통해 빛의 초점이 맺혀지는 작은 공간을 1.6 nm의 크기의 Alexa 647 단분자가 통과할 때의 움직임을 실시간으로 관측하는데 성공하였다(그림 2). 더 나아가 연구팀은 FCS 분석을 통해 분자의 확산 속도, 용액의 점도를 알 수 있고, 또한 서로 다른 크기의 미세 입자들을(퀀텀닷 및 나노입자) 구분할 수 있는 기술을 구현하였다(그림 3). 이러한 메타렌즈를 통해 휴대용 단분자 측정 시스템에 대한 가능성이 처음으로 증명되었고, 향후 후속 연구를 통해 스마트폰 현미경 및 3D 프린팅된 초소형 현미경에 메타렌즈를 결합해 휴대용 단분자 측정 시스템을 실현하고자 한다. 궁극적으로는 이러한 메타렌즈와 실리콘 포토닉스 칩이 결합된 온-칩 단분자 측정 센서가 개발될 수 있을 것으로 기대된다. 본 연구 결과는 국제학술지인 Nature Communications(IF = 16.6)에 1월 2일 정식 출판되었다. 본 연구는 뇌과학 선도융합기술개발사업, 미래유망융합기술 파이오니어 사업, ERC 선도연구센터, RLRC 지역혁신 선도연구센터, 나노커넥트, 포스코 산학연 융합연구소 사업 및 세종과학펠로우십 사업 등을 통하여 수행되었다. ※ 논문명: Dual-wavelength metalens enables epi-fluorescence detection from single molecules ▲ 그림1. 메타렌즈 기반 단분자 측정 시스템 모식도 ▲ 그림2. 메타렌즈를 통해 측정된 Alexa 647 단분자 측정 결과 그래프 ▲ 그림3. 메타렌즈로 측정된 다양한 단일 미세 입자 구분 기술
- No. 254
- 2024-02-14
- 5883
-

식품생명공학과 우한민 교수
‘RNA 유전자 가위’로 미생물 세포공장개발에 속도 낸다
식품생명공학과 우한민 교수 연구팀은 dead Cas13a RNA 유전자 가위로 박테리아에서 존재하지 않는 RNA 간섭시스템*을 개발했고, 자동화 바이오파운드리기술**을 적용하여 세포공장을 효율적으로 개발 할 수 있었다고 11월 30일 밝혔다. *RNA 간섭시스템(RNA interference): small RNA 및 messenger RNA등 RNA의 원래 기능을 제한할 수 있는 시스템으로, 다양한 유전자의 조절에 관여함. **바이오파운드리: 주문자 반도체 생산시스템과 유사하게, 생물시스템을 디자인하고 자동화 장비를 활용하여 고속으로 합성생물학 부품 및 세포공장을 개발할 수 있는 바이오제조 핵심 자동화 시설(예: 성균관대 바이오파운드리). 세포공장은 지속가능한 바이오 연료, 의약학 및 식품 소재, 화학 소재를 생산할 수 있는 산업용 박테리아로, 다양한 합성생물학 도구를 활용하여 유전자 발현을 조절하고, 대사흐름을 제어하여 세포공장의 소재 생산성을 극대화 시킬 수 있다. 이번 연구는 RNA를 자르는 효소적 기능만 상실된 dead Cas13a (dCas13a) RNA 유전자 가위를 이용하여, 박테리아 세포내 존재하는 다양한 small RNA*의 발현을 억제하는 기술을 개발하였다. 이를 통하여 기존의 기술로 제어할 수 없었던 박테리아 내 트랜스-스몰 RNA와 시스-스몰 RNA를 제어할 수 있는 원천 기술을 획득하였다. 이번 개발 기술은 고등 생물에 존재하는 RNA 간섭기술과 유사한 기술로, 박테리아에서도 고도의 유전자 발현을 제어할 수 있을 의미 한다. *small RNA는 non-coding RNA로 세포내 다양한 환경에서 특정 유전자의 발현을 조절하는 핵심적 기능을 갖고 있는 200 bp 이하의 짧은 RNA이다. 또한, 모듈러 루프 가이드 RNA를 추가로 개발하여, 타겟 RNA 발현을 66%에서 92%까지 다양하게 억제할 수 있는 기술을 확보하였으며, 이 응용 기술을 활용하여 박테리아에 많이 존재하는 폴리시스트로닉 유전자의 발현에 적용하였다. 그 결과, 기존 CRISPRi 유전자 저해 기술로 가능할 수 없었던 폴리시스트로닉 개별 유전자의 억제도 가능하게 되어, 세포공장을 효과적으로 개발할 수 있는 원천 기술을 제공하게 되었다. 더 나아가 이번 RNA 유전자 가위의 박테리아 RNA 간섭기술을 활용하여, 항산화제로 사용될 수 있는 라이코펜 생산 세포공장 개발에 적용하였으며, 바이오파운드리기술을 활용하여 알려진 93개의 대장균의 sRNA를 로봇으로 제작하고, 그 라이브러리 중 라이코펜의 생산성을 향상 시킬 수 있는 신규 타겟 sRNA를 스크리닝 할 수 있게 되었다. 따라서 대사반응에 직접 관여하는 효소 유전자의 발현 조절만 개발하던 기존 대사공학 접근법을 넘어서, 타겟 sRNA를 통한 하위 유전자의 발현을 조절하는 새로운 대사공학 접근법을 제시할 수 있었다. 이번 연구를 통하여 박테리아 RNA 간섭 기술과 함께 바이오제조의 핵심 기술인 바이오파운드리기술로 대규모 가이드 RNA를 제작하고, 세포공장용 박테리아를 형질 전환하고, 타겟 물질을 스크리닝 하여 일련의 DBTL* 과정을 자동화하여 세포공장 개발의 가속화 할 수 있었다. *DBTL: 합성생물학의 연구 철학인 Design-Build-Test-Learn Cycle을 의미한다. 우한민 교수(바이오파운드리 연구센터장)는 “이번 박테리아 RNA 간섭 원천기술과 바이오파운드리기술을 확보한 만큼 첨단 합성생물학기술을 통한 다양한 난제를 해결하고 새로운 의료 및 식품 분야, 고부가 소재 생산 분야에 적용할 수 있는 세포공장 개발에 앞서겠다.”고 설명했다. 한편 이 연구결과는 11월 28일 세계적 학술지인 ‘Nucleic Acids Research’를 통해 온라인판으로 공개됐다. 이번 연구성과는 한국연구재단이 지원하는 중견연구자지원, 기초연구실지원사업, 미생물 제어 및 응용 원천기술개발사업 및 과기정통부가 지원하는 석유대체 친환경 화학기술개발사업의 바이오화학산업 선도를 위한 차세대 바이오리파이너리 원천기술 개발 과제의 지원을 받아 수행되었다. 해당 원천기술은 국내 특허 등록이 2022년 완료되었다(특허등록번호 10-2422842). ※ 저널: Nucleic Acids Research (2023), Impact factor 14.9 (2022년 기준), JCR 생화학 및 분자생물학 분야 상위 3.3% 저널 ※ 논문제목: CRISPR-dCas13a system for programmable small RNAs and polycistronic mRNA repression in bacteria ※ DOI: 10.1093/nar/gkad1130 ※ 제1저자: 고숭천 박사(성균관대학교 식품생명공학과) ※ 교신저자: 우한민 교수(성균관대학교 식품생명공학과, 바이오파운드리연구센터, 메타바이오헬스학과) RNA 유전자 가위를 이용한 박테리아 RNA 개발과 세포공장 개발 가속화
- No. 253
- 2024-02-05
- 4210
-

성균나노과학기술원 이진욱 교수 ·박건우 연구원
페로브스카이트 태양전지 양산화의 걸림돌,낮은 공정 재현성 원인 규명
성균나노과학기술원 (SAINT) 나노과학기술학과 및 나노공학과 이진욱 교수 연구팀은 페로브스카이트 태양전지 제작 공정에서 대기습도가 페로브스카이트 박막 제작 공정 재현성과 박막 품질에 결정적인 역할을 함을 규명하였다. 해당 연구 논문은 재료과학 분야 세계 최상위 학술지인 'Advanced Materials'지에 2023년 12월 21일자로 온라인 출판되었다. 페로브스카이트 태양전지는 높은 에너지 변환 효율과, 저렴한 용액 공정을 통해 생산이 가능하여 향후 탄소 중립 실현을 위한 차세대 태양전지 기술로 각광받고 있다. 국내외 학계 및 산업계에서 상용화를 위한 활발한 연구가 매우 활발하게 진행되고 있다. 하지만, 용액 공정을 활용한 실험에서 발생하는 공정 재현성 문제는 학계 및 산업계 연구개발 과정에서 개발속도를 지연하는 주요 요소로 작용하고 있으며, 향후 양산화 과정에서 태양전지 제품의 수율을 저하시키는 주요 이슈로 작용할 것으로 보인다. 하지만 이러한 공정 재현성 저하의 원인에 대한 체계적인 연구는 그동안 수행된 바가 없었다. 연구팀은 현재 고효율 페로브스카이트 태양전지 박막 제조 과정에서는 널리 사용되는 소재를 활용한 공정에서 재현성이 저하되는 원인으로서 대기중의 습도가 결정적인 역할을 함을 규명하였다. 미국 버클리 국립 연구소 및 UCLA연구팀과의 공동연구를 통해 공정 중 습도에 따라 코팅 중 박막 내 페로브스카이트 상 핵 생성과 열처리 중 첨가제의 휘발 속도가 지대한 영향을 받음을 확인하였다 (성균관대학교 박건우 박사과정 파견연구 수행). 더 나아가, 대기 중 습도가 페로브스카이트 제조 공정에서 피해야 할 민감하고 유해한 요소라는 기존의 고정관념과는 달리, 일부 공정 중에는 일정 수준 이상의 습도가 박막 결정성 향상 및 결함 농도 감소에 도움이 될 수 있음을 제시하였다. 연구팀의 연구결과는 향후 고효율, 장수명 태양전지 개발을 위한 단서를 제공할 뿐만 아니라 페로브스카이트 태양전지 대량 양산화를 위해 그동안 다뤄지지 않았던 공정 재현성 및 수율 문제의 중요성을 최초로 제시하였다. ※ 관련 논문 및 홈페이지 1) Atmospheric Humidity Underlies Irreproducibility of Formamidinium Lead Iodide Perovskites, Advanced Material, 2023, https://doi.org/10.1002/adma.202307265 (제 1저자: 박건우 박사과정, 교신저자: 이진욱 교수) 2) 이진욱 교수 연구실 홈페이지: https://jwlee870217.wixsite.com/mysite 그림1. 페로브스카이트 박막 코팅 및 열처리 공정 중 대기습도에 따른 결정 핵 생성 변화 및 소자 효율 변화
- No. 252
- 2024-01-24
- 5703
-

의학과 및 메타바이오헬스학과 이성현 교수
RNA 비표적 효과를 줄인 미토콘드리아 염기 교정 효소 및 동물 유전질환 모델 개발
의학과 정밀의학교실 및 메타바이오헬스학과 이성현 교수는 세계 최초로 미토콘드리아 DNA의 특정 서열에서 아데닌 염기를 구아닌으로 변형한 생쥐를 제작하는 데 성공했다. 해당 연구는 연세대학교 의과대학, KIST 뇌과학연구소, 고려대학교 의과대학 및 주식회사 엣진과의 공동 연구를 통해 이루어졌다. 세포 내에 존재하는 에너지 공급원, 미토콘드리아는 그 내부에 에너지대사에 필수역할을 하는 단백질의 유전정보를 가진 미토콘드리아 DNA를 가지고 있다. 이 DNA의 결함은 미토콘드리아의 고장으로 이어지게 되며, 뇌, 신경, 근육에서 다양한 병증으로 나타나게 된다. 또한 부모 중 모계 유전으로만 전달되는 미토콘드리아의 특성상 엄마의 미토콘드리아 결함이 자녀에게 유전되어 미토콘드리아 질환으로 나타날 수 있다. 현재 크리스퍼 유전자 가위 (CRISPR-Cas9) 기술이 DNA 교정 기술로 활용되지만, 특정 DNA 서열을 인식하는 것에 사용하는 가이드 RNA가 미토콘드리아 내부로 수송되지 못하기 때문에 미토콘드리아 DNA 교정에는 사용하지 못한다는 한계점이 존재한다. 이에 대해 현재까지 개발된 미토콘드리아 DNA 교정 기술로는 DNA 염기 서열 4종류 A, G, T, C 중 C를 T로 교정 가능한 DdCBE(Nature, 2020)와 A를 G로 교정 가능한 TALED(Cell, 2022)가 있다. 이 중 DdCBE를 활용하여 미토콘드리아 C-to-T 유전자 교정을 일으킨 생쥐를 제작한 연구 사례는 있지만, 미토콘드리아 A-to-G 유전자 교정을 동물실험에서 성공한 사례는 아직까지 보고되지 않았다. 연구진은 기존에 개발된 미토콘드리아 DNA 교정 기술 TALED가 세포 내에서 의도하지 않은 무작위적 DNA 및 RNA 변형을 일으킨다는 것을 확인했으며, 이로 인해 TALED가 생쥐의 수정란에 주입될 경우 배아 발달이 정상적으로 이루어지지 못함을 발견했다. 또한 TALED 구성 단백질 중 DNA 변형을 매개하는 단백질이 더욱 정밀한 활성을 나타낼 수 있게 개량한 TALED(V28R-TALED)를 개발했으며, 이를 통해 TALED의 부작용인 세포 내 무작위적 DNA 및 RNA 변형이 크게 감소된 것을 확인했다. 나아가 개량된 TALED를 생쥐의 수정란에 미세주입해 미토콘드리아 질환 중 리 증후군(Leigh syndrome)의 돌연변이를 보유, 병증을 나타내는 생쥐를 제작하는 것에 성공했다. 이번 연구는 세계적 국제학술지인 셀<Cell>(IF=66.85)>에 2024년 1월 4일 (한국시간)에 게재되었다. 논문명: Engineering TALE-linked deaminases to facilitate precision adenine base editing in mitochondrial DNA DOI: https://doi.org/10.1016/j.cell.2023.11.035 저자: 이성현 (교신저자, 성균관대학교 의학과 및 메타바이오헬스학과 조교수) 그림 개선 된 TALED의 모식도 및 작용 방식
- No. 251
- 2024-01-15
- 5349